Паркинсонизм и его основные нозологические формы
Болезнь Паркинсона (БП) – хроническое, неуклонно прогрессирующее заболевание центральной нервной системы.
Болезнь Паркинсона (БП) – хроническое, неуклонно прогрессирующее заболевание центральной нервной системы с дегенерацией нигростриарных нейронов и нарушением функции базальных ганглиев. Она относится к одним из наиболее частых нейродегенеративных заболеваний, которые стоят на третьем месте среди причин смертности после сердечно-сосудистых и онкологических заболеваний.
Паркинсонизм известен давно, первые сообщения о лечении похожих расстройств были сделаны 1000-2500 лет до н.э.
Первое клиническое описание принадлежит английскому врачу Джеймсу Паркинсону, который опубликовал в 1817 году «Эссе о дрожательном параличе».
Подробный клинический анализ комплекса патологии был сделан в 1879 г. знаменитым французским неврологом Жаном Мартеном Шарко.
В настоящее время в классификации паркинсонизма выделяют:
I. Болезнь Паркинсона (она составляет около 70-80% всех регистрируемых случаев).
II. Вторичный (симптоматический) паркинсонизм (около 15%) включает следующие варианты: лекарственный, токсический, постгипоксический, энцефалитический, травматический, при объемных процессах, при гидроцефалии, сосудистый.
III. Паркинсонизм при различных дегенеративных заболеваниях с поражением экстрапирамидной системы («паркинсонизм-плюс», около 10%): мультисистемные атрофии (стриатонигральная дегенерация, оливопонтоцеребеллярная дегенерация), прогрессирующий надъядерный паралич (болезнь Стила-Ричардсона-Ольшевского), кортикобазальная дегенерация, деменция с тельцами Леви, паркинсонизм-БАС-деменция, болезнь Вильсона-Коновалова, болезнь Гентингтона (ювенильный вариант Вестфаля), болезнь Фара (идиопатическая кальцификация базальных ганглиев), болезнь Альцгеймера, другие.
Основной нозологической формой паркинсонизма является болезнь Паркинсона.
Этиология БП неизвестна. В основе ее патогенеза лежит дегенерация так называемых дофаминергических нейронов. БП носит преимущественно спорадический характер, однако при наличии БП у ближайших родственников риск ее развития возрастает.
Клинические проявления БП возникают при уменьшении количества дофамина в хвостатом ядре и скорлупе не менее чем на 70%. Симптомы БП развиваются постепенно, вовлекая сперва конечности на одной стороне. Для клинической картины БП характерно сочетание гипокинезии, ригидности, тремора покоя, и постуральных нарушений.
Гипокинезия проявляется снижением двигательной активности, замедленностью движений, уменьшением амплитуды действий.
Тремор покоя в классических случаях начинается с дистальных отделов верхней или нижней конечности и напоминает движения рук «при счете монет или скатывании пилюль». В дальнейшем в тремор вовлекается гомолатеральная конечность, нижняя челюсть, противоположные конечности. Иногда отмечается постуральное дрожание рук.
Кроме двигательных нарушений, при БП части развиваются недвигательные проявления: нервно-психические расстройства; нарушения сна; вегетативные нарушения; чувствительные нарушения.
В зависимости от преобладания того или иного симптома в клинической картине БП принято выделять следующие клинические формы заболевания: дрожательную, акинетическую, а также смешанные формы — акинетико-ригидную и ригидно-дрожательную.
На поздних стадиях БП клиническая картина видоизменяется, появляются дополнительные моторные (двигательные флуктуации, лекарственные дискинезии, нарушения ходьбы, падения, застывания и акинетические кризы) и немоторные (вегетативные, когнитивные, нейропсихические) синдромы.
У больных могут возникать длительные периоды декомпенсаций — от нескольких дней до нескольких недель, а также акинетические кризы — тяжелые эпизоды акинезии, сопровождающиеся дисфагией, вегетативными нарушениями, гипертермией, олигурией, спутанностью сознания. Причинами этого могут являться: нарушение схемы приема противопаркинсонических средств, их полная отмена («лекарственные каникулы»); прием препаратов, блокирующих ДА-рецепторы (прежде всего нейролептики); обострение сопутствующих соматических заболеваний, стресс; операции, травмы, дегидратация организма.
Диагностировать БП с уверенностью можно только с помощью аутопсии. Клиническая диагностика синдрома паркинсонизма требует обязательного наличия гипокинезии и не менее одного из трех основных симптомов паркинсонизма: тремора покоя, ригидности и постуральной неустойчивости.
Проведение МРТ головного мозга является обязательным при наличии у больного синдрома паркинсонизма. Данное исследование прежде всего необходимо для дифференцирования идиопатической болезни Паркинсона и вторичного паркинсонизма, а также «паркинсонизма-плюс».
Основными направлениями лечения БП являются:
1. Фармакотерапия.
2. Медико-социальная реабилитация.
3. Лечебная физическая культура (ЛФК).
4. Нейрохирургическое лечение.
Фармакотерапия при БП направлена на нормализацию биохимического дисбаланса и требует постоянного приема лекарственных средств, так как при прекращении лечения симптомы БП возвращаются к исходному уровню.
На ранней стадии лечение БП заключается в назначении монотерапии с последующим переходом на комбинированное лечение.
На ранних стадиях заболевания общепринятым является назначение больным в возрасте до 70 лет агонистов ДА-рецепторов и ингибиторов МАО-В в виде монотерапии или сочетания.
У пациентов старше 70 лет, когда ожидаемая продолжительность жизни больного меньше, а также имеются когнитивные нарушения, терапию можно сразу начинать с ДОФА-содержащих препаратов в минимальной эффективной дозе, которую подбирают постепенно.
Холинолитики (Циклодол, Акинетон) назначаются преимущественно на ранней стадии БП — в виде монотерапии или в комбинации с другими противопаркинсоническими средствами; они преимущественно влияют на тремор покоя.
В настоящее время их назначают лишь молодым пациентам, с выраженным тремором покоя и сохранными когнитивными функциями. Высокая частота побочных эффектов и низкая эффективность по сравнению с другими группами существенно ограничивают их применение.
Препараты амантадина (Мидантан, ПК-Мерц).
Амантадины могут назначаться как при начальной стадии в виде монотерапии, так и в комбинации с другими противопаркинсоническими средствами на поздних стадиях БП. Препараты эффективны и для уменьшении степени выраженности дискинезий, вызванных приемом леводопы. Инфузионная форма амантадина сульфата (ПК-Мерц) применяется при лечении декомпенсаций и акинетических кризов при БП.
Агонисты дофаминовых рецепторов обладают способностью непосредственно стимулировать ДА рецепторы в головном мозге. Неэрголиновые агонисты ДА-рецепторов (Проноран, Мирапекс, Реквип Модутаб, Ньюпро) широко применяются на всех стадиях БП. Помимо контроля двигательных нарушений, у них выявлен антидепрессивный эффект, что очень важно, так как частота депрессивного синдрома при БП достаточно высока.
Монотерапия АДАР на ранних стадиях заболевания позволяет отсрочить назначение препаратов леводопы, а также развитие моторных флюктуаций и лекарственных дискинезий.
Ингибиторы МАО типа В (Разагилин). Назначение препаратов этой группы приводит к увеличению количества дофамина в нейронах. Также предполагается наличие у них нейропротекторного действия. Могут назначаться на ранних стадиях в виде монотерапии, а также в комбинации с леводопой.
Ингибиторы КОМТ. Ингибиторы КОМТ увеличивают биодоступность леводопы, уменьшая уровень ее неактивных метаболитов.
Ингибиторы КОМТ периферического действия не проходят ГЭБ и препятствуют метилированию леводопы в желудочно-кишечном тракте и кровеносном русле. Благодаря этому они сохраняют концентрацию леводопы на определенном уровне. К таким препаратам относится энтакапон.
Комбинация энтакапона с препаратами леводопы позволяет снизить суточную дозу ДОФА-содержащего препарата на 15–30%.
Он назначается только в комбинации с препаратами леводопы (Сталево), так как при назначении в виде монотерапии самостоятельным противопаркинсоническим эффектом не обладает.
Препараты леводопы (Мадопар, Наком, Тремонорм, Тидомет-форте, Дуэллин, Синдопа). Дофамин не проходит ГЭБ, поэтому в качестве лекарственного препарата был предложен метаболический предшественник дофамина — леводопа, которая проходит через ГЭБ и в головном мозге метаболизируется в дофамин. На сегодняшний день препараты леводопы являются наиболее эффективными лекарственными средствами, «золотым стандартом», применяющимися для лечения БП. Однако они не останавливают прогрессирование БП. Более того, в среднем после 5 лет применения ДОФА-содержащих средств у больных БП снижается их эффект, появляются двигательные флюктуации и лекарственные дискинезии.
Сроки назначения терапии препаратами леводопы зависят от степени выраженности и темпа прогрессирования заболевания, профессиональной деятельности больного, семейно-бытового статуса. В целом назначать препараты этой группы необходимо, когда имеются выраженные двигательные нарушения, которые не удается купировать другими противопаркинсоническими средствами.
Нейрохирургическое лечение.
Снижение эффективности фармакотерапии, появление моторных флюктуаций и лекарственных дискинезий являются показанием к применению нейрохирургического лечения, которое в течение последних двух десятилетий прочно заняло свое место в алгоритме ведения пациентов с БП.
В настоящее время используются три типа нейрохирургических вмешательств при БП: стереотаксические деструктивные методы (вентролатеральная таламотомия, паллидотомия, субталамотомия и их комбинация), стимуляционные методы (имплантация электродов в подкорковые структуры с последующей их хронической электростимуляцией) и внутримозговая трансплантация дофаминергических нейронов мезенцефалона эмбриона человека, эффективность которой продолжает изучаться.
Наиболее современный метод хирургического лечения БП – глубокая электростимуляция головного мозга. Процедура ГСМ состоит в имплантации электродов с 4 контактами в зоны-мишени в пределах подкорковых образований головного мозга; электроды соединяются с имплантируемым под кожу стимулятором, подающим высокочастотные электрические импульсы в стимулируемое ядро.
Медико-социальная реабилитация.
Высокая степень инвалидизации при неуклонно прогрессирующей БП, социально-экономические потери, которые несет общество обусловливают необходимость создания системы медико-социальной реабилитации, которая должна включать в себя диспансерное наблюдение больных; создание школ для пациентов и их родственников ведение обучающих программ и психотерапевтических занятий, создание общественных организаций, групп поддержки.
Большое значение имеет ЛФК, которая может подбираться индивидуально в зависимости от степени тяжести болезни у конкретного больного, занятия ЛФК в группах, танцевальная терапия, а также трудотерапия, физиотерапия.
Неотложные состояния при болезни Паркинсона
Болезнь Паркинсона (БП) – хроническое прогрессирующее заболевание головного мозга, преимущественно связанное с дегенерацией дофаминергических нейронов черной субстанции с накоплением в них белка α-синуклеина и образованием особых внутриклеточных включений (телец Леви), которое проявляется сочетанием гипокинезии с ригидностью, тремором покоя и постуральной неустойчивостью, а также широким спектром немоторных проявлений (психических, вегетативных, сенсорных и др.) [1, 2].
Хроническое медленно прогрессирующее течение процесса при этом заболевании может меняться с развитием острой декомпенсации БП – внезапного нарастания симптомов паркинсонизма, сопровождающегося
существенным ограничением функциональных возможностей пациента и сохраняющегося более 24 часов, несмотря на продолжение или возобновление привычной для пациента противопаркинсонической терапии [3]. Данное расстройство развивается у 0,3-1% больных БП ежегодно, а в 10% случаев приводит к летальному исходу.
— акинетический криз (АК);
— акинетико-гипертермический (злокачественный) синдром (АГС);
— злокачественный нейролептический синдром (ЗНС);
— тяжелые инвалидизирующие дискинезии с гипертермией;
— психоз;
— серотониновый синдром (СС).
Неотложные состояния при БП, в зависимости от состояния и степени вовлеченности дофаминергической системы, условно можно разделить на две группы:
1. Неотложные состояния, возникающие в результате дофаминергического дисбаланса:
А – развивающиеся в период «OFF» или гипофункции дофаминергической системы: синдром паркинсонизм – гиперпирексия или акинетический криз;
Б – развивающиеся в период «ON» или избыточной активности дофаминергической системы: психоз, тяжелая дискинезия с гиперпирексией и т.п.;
2. Неотложные состояния, не связанные напрямую с состоянием дофаминергической системы (серотониновый синдром, электролитные нарушения и т.п.)
Акинетический криз и акинетико-гипертермический (злокачественный) синдром
Акинетический криз – резкое нарастание гипокинезии и ригидности с развитием обездвиженности, спутанности сознания, анартрии, нарушения глотания и вегетативными расстройствами (тахикардия, артериальная
гипотензия, недержание мочи, потоотделение). Для акинетико-гипертермического синдрома характерны симптомы акинетического криза, а также гипертермия (гиперпирексия), вызванная дисфункцией гипоталамуса.
К основным причинам развития АК и АГС относятся:
— изменение дофаминергической терапии;
— блокада дофаминергических рецепторов;
— интеркуррентные состояния;
— нарушение работы системы глубокой электростимуляции (при наличии таковой у пациента).
Точная частота развития АК и АГС не известна. Наиболее цитируемой работой, в которой обсуждается частота встречаемости данных расстройств, является статья M.Serrano-Duenas [4]. Согласно его данным, у 3,6% (11 пациентов из 305) регулярно наблюдаемых им пациентов с БП в течение 9 лет развилось данное расстройство. Среди всех осмотренных за 9 лет пациентов с БП данный процент составил 0,04%. Во всех случаях причиной развития АГС являлась самостоятельная отмена препаратов леводопы без согласования с лечащим врачом. С другой стороны, в исследовании ELLDOPA [5], в которое были включены пациенты с ранней стадией заболевания, в результате двухнедельной отмены леводопы ни у одного из 361 пациента не развился АГС. Данный факт указывает на значение выраженности дегенерации нигростриатного пути, отражающего стадию заболевания в развитииакинетического криза.
Патофизиология акинетического криза окончательно не ясна, однако очевидно, что в основе его развития лежит не только отмена препарата. Особенностью АК является низкая эффективность возобновленной терапии
леводопой, при этом срок начала ответа может достигать 11 дней. Таким образом, во время акинетического криза, по-видимому, развивается временная блокировка ответа на привычную для пациента терапию. В 2014 г. была опубликована работа [6], в которой при помощи SPECT с лигандом [123I] FP-CIT, проведенной до, в период и после акинетического криза, было показано, что в острый период происходит значимое снижение накопления лиганда в пресинаптических терминалях стриатума и его дальнейшее медленное восстановление.
Впервые АГС был описан в 80-е годы ХХ в. у пациентов во время прекращения дофаминергической терапии в рамках проведения «лекарственных каникул». В настоящее время, в связи с пониманием всей опасности «лекарственных каникул», наиболее частой причиной развития АК и АГС называют изменение схемы ранее назначенной терапии (резкое снижение дозы, непропорциональная замена дофаминергического препарата). Прием препаратов, блокирующих дофаминовые рецепторы, таких как типичные нейролептики, метоклопромид, циннаризин, резерпин и др., также может приводить к развитию декомпенсации БП. Более того, существуют сообщения о развитии АК на фоне приема препаратов из группы атипичных нейролептиков. Нельзя забывать и о возможности влияния интеркуррентных заболеваний на течение БП. АГС может развиваться у пациентов с патологией желудочно-кишечного тракта в связи со снижением всасывания дофаминергических препаратов и развития состояния, эквивалентного отмене терапии. К таким состояниям относятся опухоли, резекция кишечника, тяжелые гастроэнтериты, непроходимость. Некоторые сопутствующие заболевания, несмотря на отсутствие прямого влияния на всасывание препаратов, также способны приводить к АК/АГС (инфекции, дегидратация, электролитные расстройства). Основными электролитными расстройствами, способными привести к развитию острой декомпенсации, являются гипо- и даже гипернатриемия, а неадекватная коррекция данных состояний способна вызвать понтинный или экстрапонтинный миелинолиз, усугубив течение АГС. Описаны случаи развития декомпенсации, связанные с менструальным циклом – вероятно за счет отрицательного влияния высокого уровня прогестерона на дофаминергическую систему. В связи с активным внедрением глубокой электростимуляции головного мозга, нельзя забывать о возможности развития декомпенсации у пациентов, перенесших данное оперативное лечение. Акинетический криз может развиться в случае прекращения стимуляции, некорректного программирования стимулятора, разрядки батареи, и даже непреднамеренного отключения стимуляции самим пациентом. При этом описаны случаи развития АГС в результате снижения дозы дофаминергической терапии даже на фоне эффективной глубокой электростимуляции.
Акинетический криз и акинетико-гипертермический синдром – неотложные состояния, требующие срочной госпитализации пациента в отделение интенсивной терапии. При развитии данной патологии в кратчайшие сроки должна быть проведена диагностика возможных интеркуррентных заболеваний (в первую очередь инфекционных), проведен комплекс лабораторных обследований (в первую очередь для исключения водно-электролитного и кислотно-щелочного расстройства). Акинетический криз требует тесного взаимодействия реаниматолога и невролога.
Клиническая картина АГС характеризуется следующими симптомами:
— сроки развития от 18 часов до 7 суток (с момента изменения/прекращения дофаминергической терапии или развития состояния, которое могло спровоцировать декомпенсацию);
— выраженная ригидность/акинезия;
— вегетативные расстройства (тахикардия, тахипноэ, лабильность АД, нарушение мочеиспускания, цианоз, потоотделение);
— через 72-96 часов (в некоторых случаях одновременно с дебютом акинезии) развивается гипертермия (до 41 °С);
— нарушение сознания (от возбуждения до оглушения и комы);
— возможно развитие генерализованных тонико-клонических судорог, миоклоний;
— изменение лабораторных показателей: лейкоцитоз, повышение уровня креатинкиназы (260-50000 Ед/л);
Основными осложнениями АК и АГС являются:
— тромбоз глубоких вен;
— эмболия легочной артерии;
— аспирационная пневмония;
— почечная недостаточность.
Мероприятия, проведение которых необходимо при поступлении больного с акинетическим кризом:
— интубация, проведение ИВЛ (при выраженной дыхательной недостаточности);
— постановка назогастрального зонда, мочевого катетера;
— антибиотикотерапия (в случае выявления инфекционного процесса);
— назначение антипиретиков;
— адекватная инфузионная терапия (коррекция электролитных расстройств);
— гемодиализ (при выявлении почечной недостаточности);
— гепаринотерапия, компрессионный трикотаж (профилактика тромбоза глубоких вен голеней и эмболии легочной артерии);
— позиционирование в кровати (профилактика пролежней).
Основой терапии акинетического криза является восстановление приема дофаминергической терапии в случае ее отмены. Особенности ответа на возобновленную терапию требуют учета следующих аспектов:
— раннее возобновление дофаминергической терапии;
— увеличение исходной дозы дофаминергических препаратов;
— продолжение терапии вне зависимости от наличия ответа (должный ответ может развиться лишь спустя 11 суток);
— невозможность ограничения терапии акинетического криза только дофаминергическими препаратами.
Важным дополнением к терапии является введение раствора амантадина сульфата как препарата, способного снизить активность глутаматной системы, возможно лежащей в основе АГС. Следует придерживаться следующей схемы назначения препарата:
— 500 мл раствора (200 мг амантадина сульфата) 2-3 раза в день в течение 10-14 дней;
— после завершения курса инфузионной терапии обязателен перевод на пероральную форму в таблетках (300-600 мг/сут).
Также в качестве дополнительной терапии рассматриваются апоморфин, дантролен и метилпреднизолон. К сожалению, первые два препарата не зарегистрированы в нашей стране. Метилпреднизолон назначается в дозе 1000 мг/сут в течение 3-5 дней. Терапия метилпреднизолоном существенно улучшает исходы и сокращает сроки акинетического криза. Окончательный механизм действия метилпреднизолона при акинетическом кризе не ясен. В экспериментальной модели на крысах было показано наличие глюкокортикоидных рецепторов на дофаминергических нейронах в вентральной области покрышки, за счет стимуляции которых возможно и развивается эффект метилпреднизолона. Имеется сообщение о применении ротиготина в виде трансдермальной терапевтической системы при акинетическом кризе [7].
Злокачественный нейролептический синдром Злокачественный нейролептический синдром – это ятрогенная, потенциально фатальная патология, которая может развиться на фоне приема любых препаратов, блокирующих дофаминергическую передачу. Чаще всего данный синдром развивается в ответ на прием типичных нейролептиков, однако описаны случаи развития ЗНС и при терапии атипичными нейролептиками. Патогенез ЗНС связан с блокадой дофаминергических структур в базальных ганглиях и гипоталамусе, иммунологическими нарушениями и повышением проницаемости гематоэнцефалического барьера, которые приводят к нейросенсибилизации организма с последующим аутоиммунным поражением ЦНС и висцеральных органов. В патогенезе ЗНС важную роль играет симпатоадреналовая и серотониновая гиперактивность.
Частота встречаемости ЗНС составляет 0,1–1% среди больных, получающих нейролептики. В данную группу попадают и пациенты с БП, течение которой осложнилось психотическими расстройствами. Чаще всего ЗНС развивается в первые дни после начала приема препарата, либо резкого увеличения его дозы. ЗНС может проявиться в любом возрасте, но чаще наблюдается у молодых мужчин. Факторами риска при ЗНС являются интеркуррентная инфекция, физическое истощение, нарушения водно-электролитного баланса (в первую очередь дегидратация), также, как и при АГС.
Клиническая картина ЗНС во многом схожа с АГС: характерно быстрое прогрессирование симптоматики с пиком в течение 72 часов, длительностью 7-14 дней. В случае ЗНС возможно купирование симптоматики без дополнительной терапии.
В 1985 г. Levenson J.L. впервые предложил критерии диагностики данной патологии [8], позже, в 1994 г., новые критерии были предложены в рамках DSM-IV:
Для ЗНС характерны изменения лабораторных показателей:
— повышение креатинкиназы (>90%);
— полиморфонуклеарный лейкоцитоз (75%);
Levenson J.L., 1985
DSM-IV, 1994
Что такое болезнь Паркинсона? Причины возникновения, диагностику и методы лечения разберем в статье доктора Полякова Т. А., невролога со стажем в 12 лет.


Определение болезни. Причины заболевания
Болезнь Паркинсона — это одно из самых распространенных нейродегенеративных заболеваний, поражающее преимущественно дофамин-продуцирующие (дофаминергические) нейроны в определенной области мозга, называемой чёрной субстанцией с накоплением в клетках белка альфа-синуклеина и особых внутриклеточных включений (телец Леви). Это заболевание — самая частая причина синдрома паркинсонизма (80% всех случаев). Распространенность болезни Паркинсона составляет около 140 (120-180) случаев на 100 000 населения. [1] Заболевание чаще всего проявляет себя после 50 лет, однако нередки случаи дебюта болезни и в более раннем возрасте (с 16 лет). Мужчины страдают немного чаще женщин.
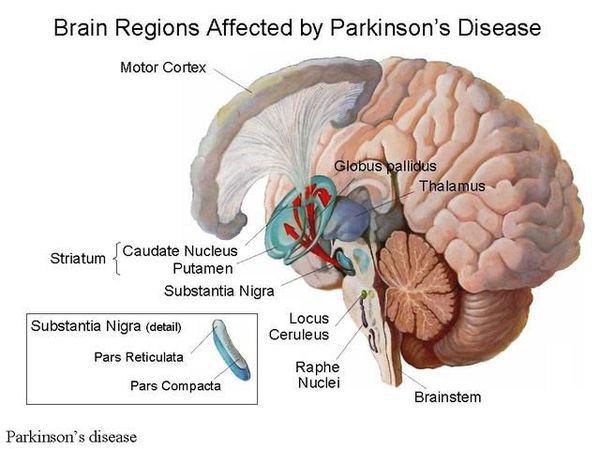
Причина остается в значительной степени неизвестной. Предполагается, что на возникновение заболевания влияют генетические факторы, внешняя среда (возможное воздействие различных токсинов), процессы старения. Генетические факторы имеют доминирующее значение при раннем развитии болезни Паркинсона. Молодые пациенты с этим заболеванием и с семейной историей болезни с большей вероятностью переносят гены, связанные с болезнью Паркинсона, такие, как SNCA, PARK2, PINK1 и LRRK2. В одном из последних исследований показано, что 65% людей с ранним началом болезни Паркинсона в возрасте до 20 лет и 32% людей с началом от 20 до 30 лет имели генетическую мутацию, которая, как полагают, увеличивает риск развития болезни Паркинсона. [2]
Симптомы болезни Паркинсона
Многие симптомы болезни Паркинсона не связаны с движением. Немоторные («невидимые симптомы») болезни Паркинсона распространены и могут влиять на повседневную жизнь больше, чем более очевидные трудности с движением. Они могут включать:
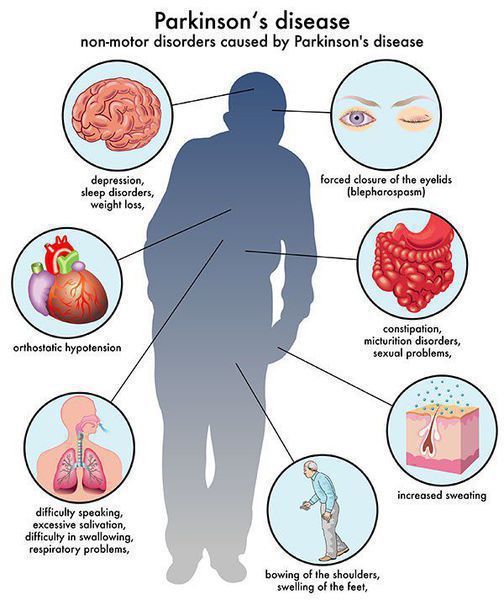
В начале заболевания нередко ставится неверный диагноз — плечелопаточный периартрит, проявляющийся болью и напряжением в мышцах руки и спины.
Синдром паркинсонизма является основным клиническим проявлением болезни Паркинсона, его симптомы: [1]
Вначале симптомы возникают только с одной стороны тела, но постепенно приобретают двусторонний характер. Симптомы остаются выраженными на той стороне, где возникли в начале заболевания. Симптомы на другой стороне тела часто не становятся такими же тяжелыми, как симптомы на начальной стороне. Движения становятся все более замедленными (основной симптом паркинсонизма). Симптомы заболевания колеблются в течения дня и зависят от многих факторов.
Патогенез болезни Паркинсона
Болезнь Паркинсона относится к группе синуклеинопатий, так как избыточное накопление в нейронах альфа-синуклеина приводит к их гибели. Повышенный уровень альфа-синуклеина может быть следствием нарушения внутриклеточной системы клиренса белков, осуществляемого лизосомамии и протеосомами. У пациентов обнаружено нарушение функционирования указанной системы, среди причин которого указывают старение, окислительный стресс, действие воспаления, токсины окружающей среды. Клетки гибнут предположительно из-за активации генетически запрограмированного механизма (апоптоза). [4]
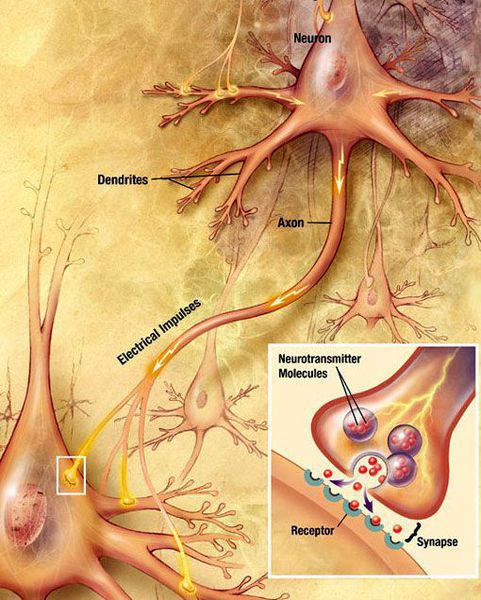
Классификация и стадии развития болезни Паркинсона
Болезнь Паркинсона классифицируется по форме, стадии и темпу прогрессирования заболевания.
В зависимости от преобладания в клинической картине того или иного симптома выделяют следующие формы: [1]
1. Смешанная (акинетико-ригидная-дрожательная) форма характеризуется наличием всех трёх основных симптомов в разном соотношении.
2. Акинетико-ригидная форма характеризуется выраженными признаками гипокинезии и ригидности, к которым обычно рано присоединяются нарушения ходьбы и постуральная неустойчивость, при этом тремор покоя отсутствует или выражен минимально.
3. Дрожательная форма характеризуется доминированием в клинической картине тремора покоя, признаки гипокинезии уходят на второй план.

Для характеристики стадий Болезни Паркинсона используется шкала Хен–Яра, 1967:
Выделяют три варианта темпа прогрессирования заболевания:
Осложнения болезни Паркинсона
Болезнь Паркинсона — не смертельное заболевание. Человек умирает с ним, а не от него. Однако поскольку симптомы ухудшаются, они могут вызвать инциденты, которые приводят к смерти. Например, в сложных случаях затруднение глотания может привести к тому, что пациенты начнут аспирировать пищу в легкие, что приведет к пневмонии или другим легочным осложнениям. Потеря равновесия может привести к падению, которое, в свою очередь, может привести к серьезным травмам или смерти. Серьезность этих инцидентов во многом зависит от возраста пациента, общего состояния здоровья и стадии заболевания.
На более поздних стадиях заболевания проявляются более выраженные симптомы болезни Паркинсона: дискинезия (непроизвольные движения или подергивание частей тела, которые могут возникнуть в результате длительного использования леводопы, застывания (внезапное отсутствие возможности двигаться) или семенящая походка (короткие, почти бегущие шаги, которые как будто ускоряются сами по себе).
Следует помнить, что болезнь Паркинсона очень индивидуальна по своему течению и у каждого протекает по своему сценарию.
Диагностика болезни Паркинсона
Паркинсонизм относится к числу тех расстройств, которые можно диагностировать на расстоянии, особенно при развёрнутой картине заболевания. Однако диагностировать болезнь Паркинсона на ранней стадии сложно. Ранняя и точная диагностика заболевания очень важна для разработки лучших стратегий лечения и поддержания высокого качества жизни как можно дольше. В практике возможна недооценка или переоценка болезни Паркинсона. Невролог, специализирующийся на расстройствах движения сможет поставить наиболее точный диагноз. Первоначальная оценка проводится на основе анамнеза, неврологического обследования с использованием специальных тестов для оценки симптомов заболевания. Неврологическое обследование включает в себя оценку координации, ходьбы и мелких моторных задач, оценку нейропсихологического статуса.
Практика получения второго мнения в значительной степени зависит от личного выбора пациента. Но имейте в виду, что болезнь Паркинсона часто трудно диагностировать точно, особенно когда симптомы незначительно выражены. Простейшего диагностического теста нет, и примерно 25% диагнозов болезни Паркинсона неверны. Болезнь Паркинсона начинается с мало видимых симптомов, поэтому многие врачи, которые не обучены в сфере двигательных расстройств, не могут поставить точный диагноз. На самом деле даже лучшие неврологи могут ошибаться. Если врач не имеет особого опыта в этой области, то необходимо консультироваться со специалистом по расстройствам движения. Хороший невролог поймет ваше желание подтвердить диагноз. Второе мнение может помочь принять своевременно правильные решения относительно диагноза и терапии.
Лечение болезни Паркинсона
Несмотря на то, что излечения болезни Паркинсона не существует, есть множество методов, которые могут позволить вести полноценную и продуктивную жизнь на многие годы вперед. Многие симптомы могут облегчаться лекарствами, хотя со временем они могут утратить свою эффективность и вызвать нежелательные побочные эффекты (например, непроизвольные движения, известные как дискинезия).
Существует несколько методов лечения, замедляющих появление моторных симптомов и улучшающих двигательные функции. Все эти методы лечения предназначены для увеличения количества дофамина в головном мозге либо путем его замещения, либо продления эффекта дофамина путем ингибирования его распада. Исследования показали, что терапия на ранней стадии может задержать развитие двигательных симптомов, тем самым улучшая качество жизни. [5]
На характер и эффективность лечения влияет ряд факторов:
Задача терапии при болезни Паркинсона — восстановить нарушенные двигательные функции и поддержать оптимальную мобильность в течение максимально длительного периода времени, сведя к минимуму риск побочных действий препаратов. [1]
Существуют также хирургические вмешательства, такие, как глубокая стимуляция мозга, подразумевающая имплантацию электродов в мозг. Из-за рисков, присущих этому типу лечения, большинство пациентов исключают данный метод лечения до тех пор, пока лекарства, которые они принимают, больше не дают им значимого облегчения. Обычно этот метод лечения проводится у пациентов с длительностью заболевания от четырех лет, получающих эффект от лекарств, но имеющих моторные осложнения, такие, как: значительное «отключение» (периоды, когда лекарство плохо работает и симптомы возвращаются) и/или дискинезии (неконтролируемые, непроизвольные движения). Глубокая стимуляция мозга лучше всего работает в отношении таких симптомов, как: скованность, медлительность и тремор, не работает с целью коррекции устойчивости, застывания при ходьбе и немоторных симптомах. Данное лечение может даже усугубить проблемы с памятью, поэтому хирургия не рекомендуется для людей с когнитивными расстройствами. [6]
Различные новые способы введения леводопы открывают дополнительные возможности терапии. Сегодня используется интестинальный (кишечный) дуодопа-гель, который уменьшает ежедневные периоды «выключения» и дискинезию у пациентов с прогрессирующей болезнью Паркинсона благодаря постоянному неимпульсному режиму введения препарата. [7]
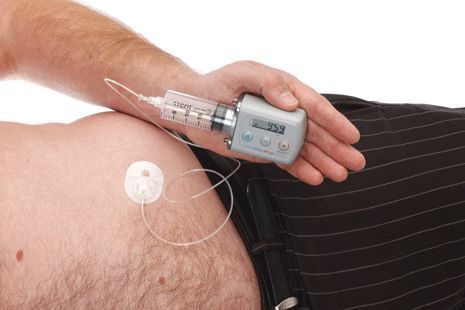
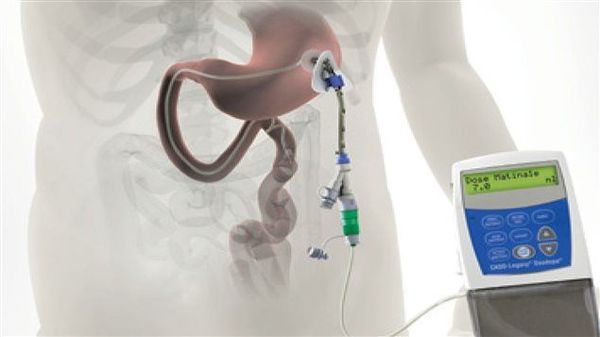
Исследуется альтернативный подход, использование допаминовых продуцирующих клеток, полученных из стволовых клеток. Хотя терапия стволовыми клетками имеет большой потенциал, требуется больше исследований, прежде чем такие клетки могут стать инструментом в лечении болезни Паркинсона. [8] [9]
По мере прогрессирования болезни Паркинсона возможности хранения и буферизации дофамина в мозге становятся все более скомпрометированными, сужая терапевтическое окно для терапии и приводя к колебаниям двигательной системы человека. Апоморфин в виде помпы доставляет подкожную инфузию в течение дня для лечения флуктуаций (феномены «ON-OFF») у пациентов с болезнью Паркинсона, которые недостаточно контролируются пероральным антипаркинсоническими препаратами. Эта система используется постоянно, чтобы обеспечить мозг непрерывной стимуляцией.
Прогноз. Профилактика
Болезнь Паркинсона уникальна для каждого человека, никто не может предсказать, какие симптомы появятся и когда именно. Существуют общее сходство картины прогрессирования болезни, но нет никакой гарантии, что то, что наблюдается у одного, будет у всех с аналогичным диагнозом. Некоторые люди оказываются в инвалидных колясках; другие все еще участвуют в марафонах. Некоторые не могут застегнуть ожерелье, в то время как другие делают ожерелья вручную.
Пациент может сделать всё, чтобы активно повлиять на течение болезни Паркинсона и, по крайней мере, на одну очень вескую причину: ухудшение симптомов часто значительно медленнее у тех, кто проявляет позитивную и активную позицию по отношению к своему состоянию, чем те, кто этого не делает. В первую очередь рекомендуется найти врача, которому доверит пациент, и который будет сотрудничать по развивающемуся плану лечения. Снижение стресса обязательно — стресс ухудшает каждый симптом болезни Паркинсона. Рекомендуются занятия образовательного направления: рисование, пение, чтение стихов, рукоделие, изучение языков, путешествия, работа в коллективе, занятия общественной деятельностью.
К сожалению, даже если адекватно подобрать медикаментозную терапию, это не гарантирует того, что клетки перестанут гибнуть при болезни Паркинсона. Терапия должна быть направлена на создание благоприятных условий для двигательной активности с учётом индивидуальных особенностей клинической картины заболевания. Как показывают результаты многочисленных исследований, профессиональная двигательная реабилитация является необходимым условием для замедления прогрессирования заболевания и улучшения его прогноза. На сегодняшний день по данным клинических исследований показана эффективность реабилитационной программы по протоколам LSVT LOUD, LSVT BIG, теоретическая основа которых сводится к развитию нейропластичности вещества мозга. Она направлена на коррекцию дрожания, ходьбы, постуры, равновесия, мышечного тонуса и речи. [10]
Реабилитационные методики должны быть направленные не только на поддержание сохранившихся двигательных способностей, но и выработку новых навыков, которые бы помогали человеку с болезнью Паркинсона преодолевать ограниченность его физических возможностей, чему способствует программа танцевально-двигательной терапии при болезни Паркинсона, работающая более чем в 100 сообществах по всему миру, включая Россию. Танцевальная терапия позволяет частично решить конкретные проблемы болезни Паркинсона: потеря равновесия, ухудшение координации, шаркающая походка, тремор, застывания, социальная изоляция, депрессия и повышенный уровень тревожности.
Согласно американскому исследованию с участием 52 больных болезнью Паркинсона, регулярная практика аргентинского танца уменьшает симптомы болезни, улучшает баланс и улучшает выполнение сложных движений при болезни Паркинсона. [11]
